에이비엘바이오 파트너사 컴패스 테라퓨틱스가 DLL4xVEGF-A 이중항체 ‘토베세믹(tovecemic, CTX-009/ABL001)’의 담도암 임상2/3상에서 1차종결점을 충족시킨 긍정적인 결과를 내놨다.
신한투자증권은 2일 컴패스의 주가가 국내 임상2상보다 낮은 수치가 발표돼 단기적으로 하락했으나 생존기간 데이터에 대한 기대감으로 전날보다 17.89% 상승해 마감했다고 분석했다.
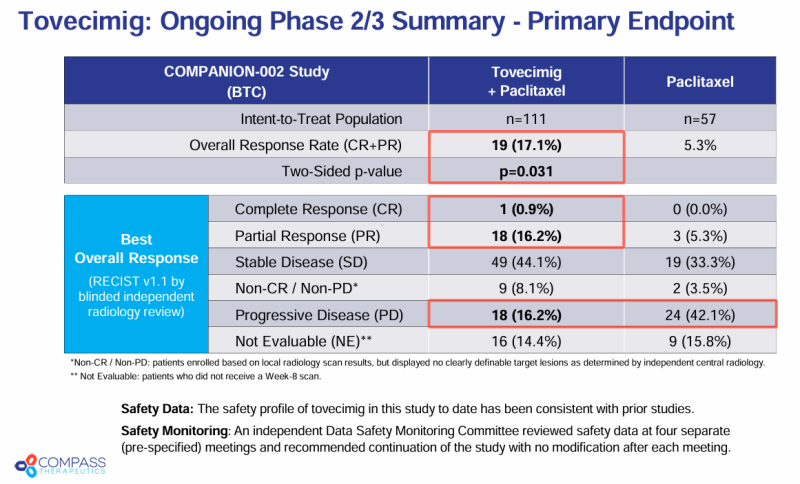
컴패스는 토베세믹을 투여한 환자군에서 전체반응률(ORR) 17.1%(19/111명) 대조군 5.3%(3/57명) 대비 3배이상 통계적으로 유의미하게 개선된 결과를 보였다(p<0.031). 특히 완전관해(CR) 환자도 1명 보고됐다.
이는 이전에 1번이상 치료받은 환자를 대상으로 진행한 임상이다. 임상에 참여한 환자는 모두 파클리탁셀을 투여받았다.
엄민용 신한투자증권 연구원은 “국내 2상 3차치료제의 ORR 15.4%와 유사해 이번 임상이 3차 이상의 환자를 대상으로 한 것으로 추정된다”고 설명했다.
회사측은 기존 2차치료제의 표준요법인 폴폭스(FOLFOX)의 ORR 4.9% 대비 3배 이상의 우월한 ORR로 시장내 Best-in-Class 약물이 될 가능할 것이라고 기대감을 보였다.
컴패스는 2차종결점인 전체생존기간(OS), 무진행생존기간(PFS), 반응지속기간(DoR) 등은 아직 성숙되지 않아 오는 3분기부터 분석을 시작할 예정이다. 결과는 4분기에 발표할 수 있을 것으로 전망했다.
신한투자증권은 이번 임상이 지난 2023년 1월 9일 환자모집이 시작돼 바로 투약이 시작됐다고 가정한다면 2년 이상 생존환자가 존재할 가능성이 있다고 분석했다.
기존 담도암에 대한 표준치료제인 ‘임핀지+젬시스’ 병용요법의 24개월 생존율은 23.6% 수준이다. 토베세믹 투여군에서 이런 생존기간의 개선 기대감이 주가에 반영됐다는 설명이다.
엄 연구원은 “올해 2분기 미국 식품의약국(FDA)와 토베세믹의 가속승인 신청관련해 논의할 예정으로 FDA 가속승인 기대감이 유지되고 있다”며 “또한 에이비엘바이오는 2~3분기 중에 발표될 사노피의 긍정적인 임상1상 데이터와 혈뇌장벽(BBB) 투과 플랫폼의 추가계약도 순항중”이라고 강조했다.
김민정 DS투자증권 연구원은 "담도암 2+차 치료제 시장은 매우 작기 때문에 ABL001의 임상 결과가 기업 가치에 미치는 영향 또한 매우 적을 것"이라며 "핵심 밸류는 사노피에 기술이전한 BBB플랫폼을 활용한 'ABL301'에 있음을 유의해야 한다"고 설명했다.