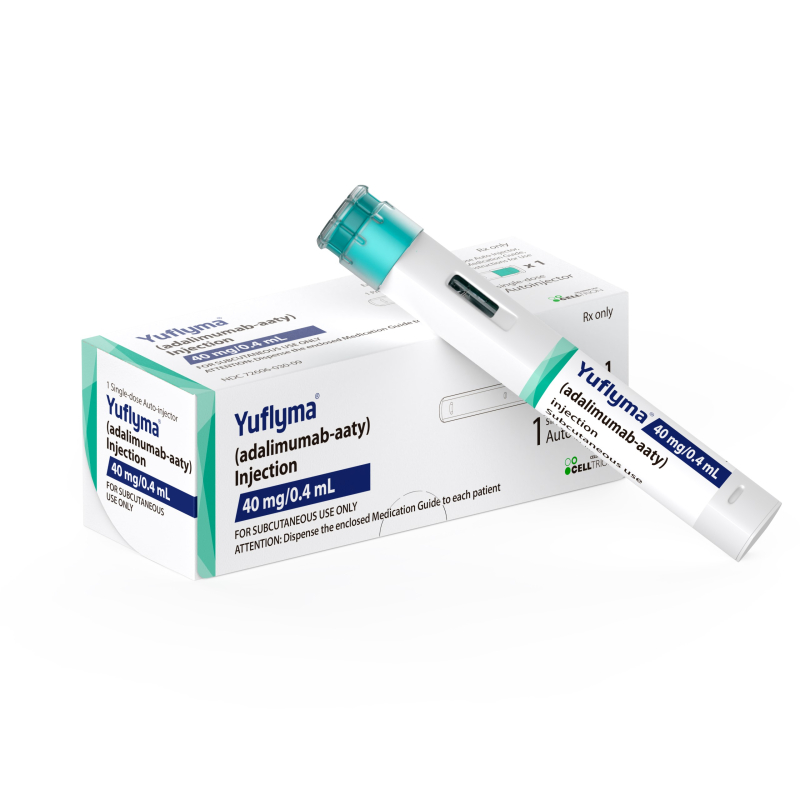
셀트리온은 4일 고농도 휴미라 '유플라이마(Yuflyma)’와 휴미라(Humira) 간 교체처방(interchangeability) 글로벌 임상 3상의 결과를 국제학술지 ‘Dermatology and Therapy’에 게재됐다고 밝혔다.
이번 논문을 통해 공개한 연구는 27주간 진행된 유플라이마와 휴미라 간 교체처방 글로벌 임상 3상을 52주까지 연장한 결과다. 연구팀은 유플라이마를 단독 투여해 오픈라벨Open-Label Extension Study)로 진행했다.
앞서 셀트리온은 중등도 내지 중증 판상형 건선 환자 367명을 대상으로 진행한 유플라이마의 글로벌 교체처장 임상3상을 진행했다. 27주차 분석에서 유플라이마와 휴미라 간의 약동학적 특성에서 통계적으로 동등성 기준에 부합한 결과를 확인했다. 또한 유효성과 안전성, 면역원성도 유사했다.
이후 27주차부터 유플라이마와 휴미라 간 다회교차 투약군과 휴미라 유지 투약군 모두 유플라이마를 단독으로 투여 받았다.
52주까지 진행된 오픈라벨 연장연구 분석결과 이전 투약과 관계없이 약동학, 유효성, 안전성, 면역원성 결과가 모두 일관되게 유지됐다. 또, 비교군 간 유사한 결과를 확인했다.
셀트리온은 지난해 1월 해당 임상 결과를 바탕으로 미국 식품의약국(FDA)에 유플라이마와 휴미라 간 교체처방을 위한 변경허가 신청서를 제출했다. 교체처방으로 승인받을 경우에는 미국 시장 점유율 확대에 긍정적인 영향을 미칠 것으로 회사측은 기대하고 있다. 미국에서는 제품명이 아닌 성분명으로 처방전이 발행되는 시스템이다.
유플라이마의 오리지널 의약품인 휴미라는 2024년 기준 89억9300만달러(한화 12조5902억원)의 매출을 기록한 글로벌 블록버스터 제품이다. 이 중 전체 매출의 79% 이상인 71억4200만 달러(한화 9조9988억원)가 미국내 매출이다.
셀트리온 관계자는 “유플라이마의 교체처방 임상결과가 연이어 저명한 국제학술지에 게재되면서 미국을 비롯한 글로벌 주요 국가에서 제품 경쟁력을 다시 한번 입증하게 됐다”며 “각 국가별 맞춤 전략으로 글로벌 시장 점유율 상승세가 지속될 수 있도록 최선을 다할 것”이라고 말했다.