유한양행 자회사 프로젠(Progen)이 GLP-1/GLP-2 이중작용제의 비만∙당뇨병 임상2상에서 내달 첫환자 투여를 시작으로 임상개발을 본격화한다.
프로젠 “GLP-1/GLP-2 이중작용제 'PG-102' 내년 하반기 임상 3상 목표”김종균 프로젠 대표는 29일 여의도 한국거래소에서 열린 2024년 코넥스시장 상장법인 합동 IR 행사에서 “비만∙당뇨병 치료제 후보물질 ‘PG-102’의 유효성을 확인(PoC)할 수 있는 임상2상 중간분석 결과는 내년 상반기 도출을 기대하고 있다”며 “내년 하반기 임상3상을 시작해 2027년까지 신약허가신청(BLA)을 제출하는 것이 목표”라고 밝혔다.
프로젠은 지난 1998년 동아제약의 자회사로 설립됐으며, 다중 표적 융합단백질 플랫폼 기술인 ‘NTIG®’를 기반으로 현재 GLP-1/GLP-2 이중작용 기전의 ‘PG-102’ 연구개발에 집중하고 있다. 프로젠의 최대주주는 유한양행으로 프로젠의 지분 34.8%를 보유하고 있다.
프로젠은 PG-102의 임상1상이 마무리단계에 진입하고 있는 상황에서 국내 14개 대학병원에서 144명의 비만∙당뇨병 환자를 모집해 임상2상을 진행할 예정이다. 프로젠은 내달 PG-102의 첫환자 투여를 계획하고 있다. 프로젠은 올해 7월 PG-102의 비만∙당뇨병 임상2상의 임상시험계획을 승인받은 바 있다.
또한 프로젠은 최근 신한투자증권과 IM증권을 공동 대표주관사로 선정하고 코스닥 시장 이전상장을 추진한다. 프로젠은 지난해 11월 코넥스 시장에 상장했다.
김 대표는 “PG-102의 PoC 데이터 기반 기술이전과 파트너십을 기반으로 내년 하반기 코스닥 상장을 위한 예비심사 청구를 진행하는 것이 목표”라고 말했다.
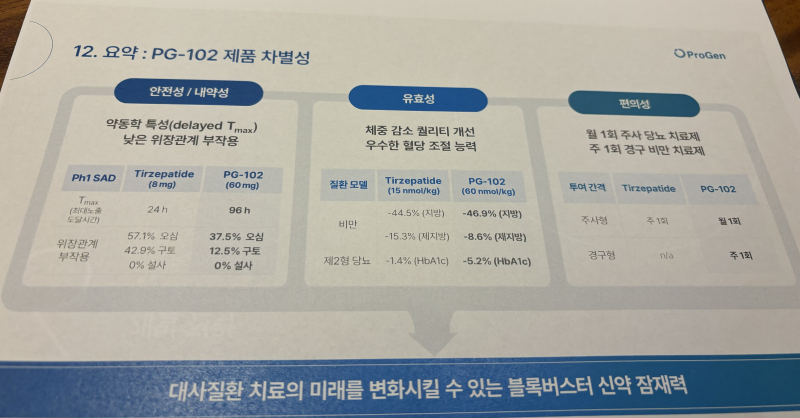
PG-102, 당뇨병 주1회 주사제형+비만 주1회 경구용 “개발전략 차별화”
프로젠은 PG-102를 당뇨병을 적응증으로 월1회 주사제형과 비만을 적응증으로 주1회 경구용 약물로 개발할 계획이다.
김종균 대표는 “치열한 경쟁이 벌어지고 있는 비만∙당뇨병 시장에서 PG-102를 월1회 주사제형 당뇨병 치료제와 주1회 경구용 비만 치료제로 포지셔닝하는 개발전략으로 차별화를 두고 있다”고 설명했다.
경구용 비만 치료제는 라니 테라퓨틱스(Rani Therapeutics)와 공동개발한다. 프로젠은 올해 6월 라니와 공동개발 계약을 맺고, 라니의 경구용 기술 ‘라니필’을 PG-102에 적용한 ‘RPG-102/RT-114’를 개발할 계획이다. 라니필은 소장에서 캡슐 내 마이크로니들을 통해 약물을 방출해 생체이용률을 높여 복용편의성을 향상시킬 수 있는 기술이다.
그는 “노보노디스크의 경구용 GLP-1 작용제 ‘리벨서스’의 생체이용률이 1% 수준으로 알려졌다”며 “라니의 기술을 적용한 경우, 34~84% 수준의 생체이용률을 보이는 것으로 알려져 있어 경쟁력이 있다고 판단한다”고 강조했다.
프로젠은 내년 상반기 주1회 경구용 비만치료제의 호주 임상1상 진입을 목표로 하고 있다.